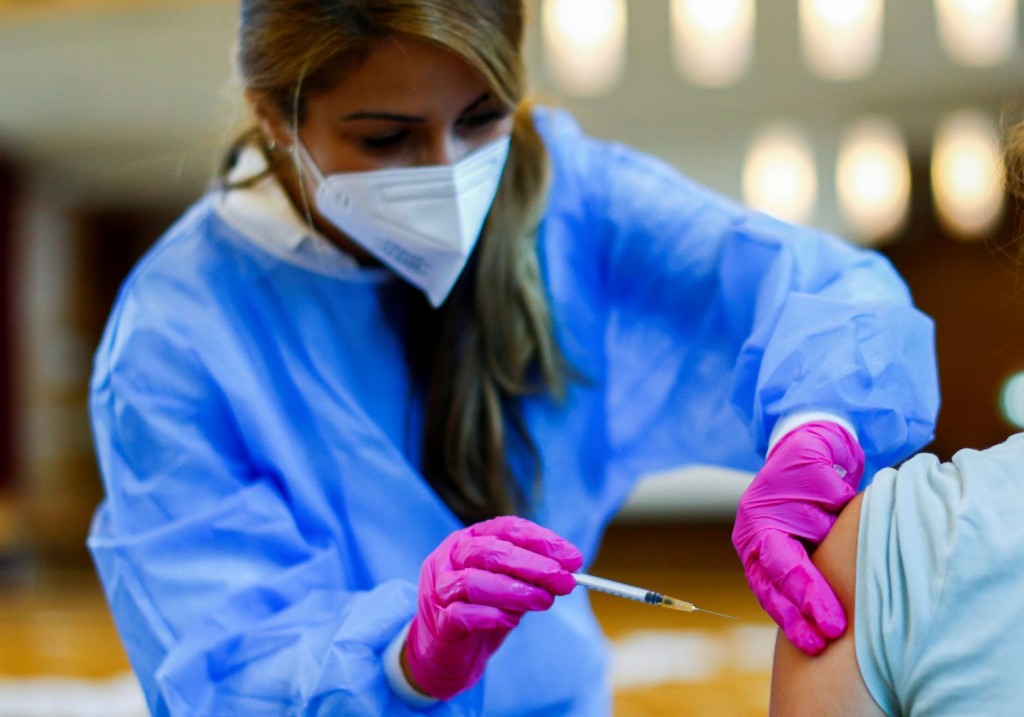
Εμβόλιο – Ξεκίνησε δοκιμή τρίτης δόσης σε ασθενείς με αυτοάνοσα νοσήματα
Στο πλαίσιο της δοκιμής που διεξάγεται από τα Εθνικά Ινστιτούτα Υγείας των ΗΠΑ θα διερευνηθεί και η προσωρινή διακοπή χορήγησης της ανοσοκατασταλτικής θεραπείας με στόχο τη βελτίωση της αντισωματικής απόκρισης
Τα Εθνικά Ινστιτούτα Υγείας των ΗΠΑ (ΝΙΗ) ξεκίνησαν κλινική δοκιμή που αφορά χορήγηση τρίτης ενισχυτικής δόσης εμβολίου για τον νέο κορωνοϊό σε ασθενείς με αυτοάνοσα νοσήματα οι οποίοι δεν είχαν καλή απόκριση στο αρχικό εμβολιαστικό σχήμα ενάντια στην COVID-19. Στο πλαίσιο της κλινικής δοκιμής αναμένεται να διερευνηθεί επίσης αν η προσωρινή διακοπή της ανοσοκατασταλτικής θεραπείας που λαμβάνουν οι ασθενείς για την αντιμετώπιση του αυτοάνοσου νοσήματός τους μπορεί να οδηγήσει σε βελτίωση της αντισωματικής απόκρισης μετά από μια επιπλέον δόση εμβολίου. Η δοκιμής φάσης 2 χρηματοδοτείται από το Εθνικό Ινστιτούτο για την Αλλεργία και τα Μεταδιδόμενα Νοσήματα (ΝΙΑΙD), ένα από τα ΝΙΗ, και διεξάγεται από ειδικούς των Κέντρων Αριστείας για την Αυτοανοσία του ΝΙΑΙD.
Φτωχή ανοσολογική απόκριση
«Πολλά άτομα με αυτοάνοσα νοσήματα τα οποία απαιτούν λήψη ανοσοκατασταλτικής θεραπείας είχαν φτωχή ανοσολογική απόκριση στα εγκεκριμένα εμβόλια για την COVID-19, με αποτέλεσμα να ανήκουν σε ομάδα υψηλού κινδύνου για σοβαρή νόσηση» ανέφερε ο διευθυντής του ΝΙΑΙD και επικεφαλής λοιμωξιολόγος στις ΗΠΑ για την αντιμετώπιση της πανδημίας του SARS-CoV-2, δρ Αντονι Φάουτσι. Ο δρ Φάουτσι προσέθεσε ότι «είμαστε αποφασισμένοι να βρούμε τρόπους ώστε να επαγάγουμε προστατευτική ανοσολογική απόκριση στα εμβόλια στον συγκεκριμένο πληθυσμό ασθενών. Η νέα αυτή μελέτη αποτελεί σημαντικό βήμα προς αυτήν την κατεύθυνση».
Υψηλός κίνδυνος για σοβαρή νόσηση
Εκτιμάται ότι ποσοστό της τάξεως του 10% του πληθυσμού πάσχει από κάποιο αυτοάνοσο νόσημα. Ερευνητές έχουν αναφέρει υψηλότερα ποσοστά σοβαρής νόσησης και θανάτου εξαιτίας της COVID-19 στα άτομα με αυτοάνοσα νοσήματα σε σύγκριση με τον γενικό πληθυσμό. Παραμένει ασαφές αν αυτό οφείλεται στο ίδιο το αυτοάνοσο νόσημα, στις ανοσοκατασταλτικές θεραπείες που λαμβάνονται για τη θεραπεία του ή και στα δύο.
Τα αποτελέσματα στους μεταμοσχευμένους ασθενείς
Αποτελέσματα πρόσφατων μελετών δείχνουν ότι η χορήγηση ενισχυτικής δόσης εμβολίου για τον νέο κορωνοϊό σε ασθενείς που έχουν υποβληθεί σε μεταμόσχευση συμπαγούς οργάνου και λαμβάνουν ανοσοκατασταλτική θεραπεία μπορεί να βελτιώσει την ανοσοαπόκρισή τους στο εμβόλιο στην πλειονότητα των περιπτώσεων. Μάλιστα βρίσκεται ήδη σε εξέλιξη σχετική μελέτη του ΝΙΑΙD στη συγκεκριμένη κατηγορία ασθενών ώστε να διερευνηθούν περαιτέρω αυτά τα πρώτα ευρήματα. Παράλληλα τα αποτελέσματα στους μεταμοσχευμένους ασθενείς μαρτυρούν ότι μια ενισχυτική δόση εμβολίου μπορεί να βοηθήσει και άτομα με αυτοάνοσα νοσήματα που λαμβάνουν κάποια συγκεκριμένα ανοσοκατασταλτικά φάρμακα. Σημειώνεται ότι η αρμόδια Υπηρεσία Τροφίμων και Φαρμάκων των ΗΠΑ (FDA) τροποποίησε προσφάτως την άδεια έκτακτης χρήσης που είχαν λάβει τα εμβόλια των Pfizer/BioNTech και της Moderna προκειμένου να επιτραπεί η χορήγηση επιπλέον δόσης στους ασθενείς που έχουν υποβληθεί σε μεταμόσχευση συμπαγούς οργάνου καθώς και σε άλλες κατηγορίες ασθενών που βρίσκονται σε αντίστοιχο επίπεδο ανοσοκαταστολής.
Ποιοι ασθενείς θα συμμετάσχουν στη δοκιμή
Η νέα κλινική δοκιμή του ΝΙΑΙD (ονομάζεται COVID-19 Booster Vaccine in Autoimmune Disease Non-Responders) θα περιλάβει αρχικώς ασθενείς με πέντε αυτοάνοσα νοσήματα: πολλαπλή σκλήρυνση, πέμφιγα (αυτοάνοσο νόσημα που προκαλεί πομφόλυγες, δηλαδή φουσκάλες στο δέρμα και στους βλεννογόνους), ρευματοειδή αρθρίτιδα, συστηματικό ερυθηματώδη λύκο, συστηματική σκλήρυνση ή σκληρόδερμα. Οι ανοσοκατασταλτικές θεραπείες που συνήθως λαμβάνονται από άτομα με αυτές τις νόσους έχουν συνδεθεί με ανεπαρκή ανοσοαπόκριση στα εμβόλια.
Στην κλινική δοκιμή αναμένεται να συμμετάσχουν περί τους 600 ασθενείς ηλικίας 18 ετών και άνω από 15-20 περιοχές των ΗΠΑ. Οι συμμετέχοντες θα πρέπει να έχουν αρνητική ή ανεπαρκή αντισωματική απόκριση μετά τη λήψη και των δύο δόσεων των εμβολίων της Μoderna ή των Pfizer/BioNTech ή του μονοδοσικού εμβολίου της Johnson & Johnson. Επίσης θα πρέπει να λαμβάνουν μια από τις τρεις ακόλουθες ανοσοκατασταλτικές θεραπείες: μυκοφαινολική μοφετίλη (MMF) ή μυκοφαινολικό οξύ (ΜΡΑ), μεθοτρεξάτη, φάρμακα που στοχεύουν στη μείωση των Β κυττάρων.
Η προσωρινή διακοπή της ανοσοκατασταλτικής θεραπείας
Ολοι οι ασθενείς θα λάβουν μια επιπλέον δόση του ίδιου εμβολίου που είχαν λάβει και αρχικώς. Ορισμένοι από αυτούς θα συνεχίσουν να λαμβάνουν την ανοσοκατασταλτική θεραπεία τους κανονικά ενώ κάποιοι θα σταματήσουν τη λήψη των ανοσοκατασταλτικών φαρμάκων για ένα μικρό χρονικό διάστημα πριν και μετά τη λήψη της επιπλέον δόσης του εμβολίου προκειμένου να φανεί αν θα έχουν καλύτερη αντισωματική απόκριση σε σύγκριση με όσους θα συνεχίσουν κανονικά τη θεραπεία τους. Ο κύριος στόχος της μελέτης είναι να προσδιοριστεί το πόσοι ασθενείς θα έχουν σημαντικά καλύτερη αντισωματική απόκριση τέσσερις εβδομάδες μετά τη λήψη της ενισχυτικής δόσης του εμβολίου σε σχέση με την αντισωματική απόκριση που είχαν παρουσιάσει μετά την ολοκλήρωση του βασικού εμβολιαστικού σχήματος.
Η κλινική δοκιμή θα διαρκέσει συνολικά 13 μήνες και τα πρώτα αποτελέσματά της αναμένονται τον προσεχή Νοέμβριο.
- Τζόουνς: «Ανυπομονώ να παίξω μπροστά στον κόσμο μας»
- Ανέβασε στα social media την καταδίωξή του από αστυνομικούς – Διέλυσε σε ανταλλακτικά τη μηχανή για να μην εντοπιστεί
- Πιερρακάκης για τους δασμούς Τραμπ: «Κλειδί ο διάλογος» – Θεμελιώδεις αρχές κυριαρχία και εδαφική ακεραιότητα
- O βασιλιάς του Μαρόκου αποδέχθηκε την πρόταση Τραμπ για ένταξή του ως ιδρυτικό μέλος στο Συμβούλιο Ειρήνης
- Australian Open 2026: Όλοι οι χορηγοί του Slam και η πραγματική αξία των συμφωνιών
- Ανί Ερνό: Όταν μια παράνομη έκτρωση κόντεψε να τη σκοτώσει, έκανε το δικαίωμα στην άμβλωση σημαία της
- Η μέρα των αποφάσεων για τις αγροτικές κινητοποιήσεις έφτασε – Το κλίμα στα μπλόκα και η αγωνία του Μαξίμου
- Χοκς – Μπακς 110-112: Νίκη – ανάσα στην Ατλάντα με «διπλό» Αντετοκούνμπο (vid)
Ακολουθήστε το in.gr στο Google News και μάθετε πρώτοι όλες τις ειδήσεις







![Άκρως Ζωδιακό: Τα Do’s και Don’ts στα ζώδια σήμερα [Δευτέρα 19.01.2026]](https://www.in.gr/wp-content/uploads/2026/01/lucas-marconnet-Kls_Hq8p-xI-unsplash-315x220.jpg)



























































 Αριθμός Πιστοποίησης Μ.Η.Τ.232442
Αριθμός Πιστοποίησης Μ.Η.Τ.232442